Rotação de Opioides: POR QUE E COMO FAZER?
IRIMAR DE PAULA POSSO CRM-SP 12.934
Ex-presidente da Sociedade Brasileira para o Estudo da Dor. Ex-professor Associado de Anestesio-logia do Departamento de Cirurgia da Faculdade de Medicina da Uni-versidade de São Paulo. Ex-profes-sor Titular de Farmacologia, Anes-tesiologia e Terapêutica da Dor da Universidade de Taubaté.
Introdução
A prescrição de opioides para o tratamento de dores crônicas oncológicas e não oncológicas habitualmente gera temor sem fundamento na maioria dos médicos, porém, esses medicamentos são responsáveis por menos efeitos adversos do que outros fármacos prescritos sem receios, em doses elevadas por períodos prolongados, como os antiinflamatórios não esteroides (AINEs) ou os anticoagulantes, por falta de formação específica, como comprova um estudo realizado nos EUA, em que apenas 20% de médicos recémformados
responderam corretamente às perguntas de escolha múltipla sobre analgesia opioide, sendo que mais da metade não sabia converter uma dose de morfina endovenosa em morfina oral¹-² .
Opióides no controle de dores crônicas oncológicas e não oncológicas
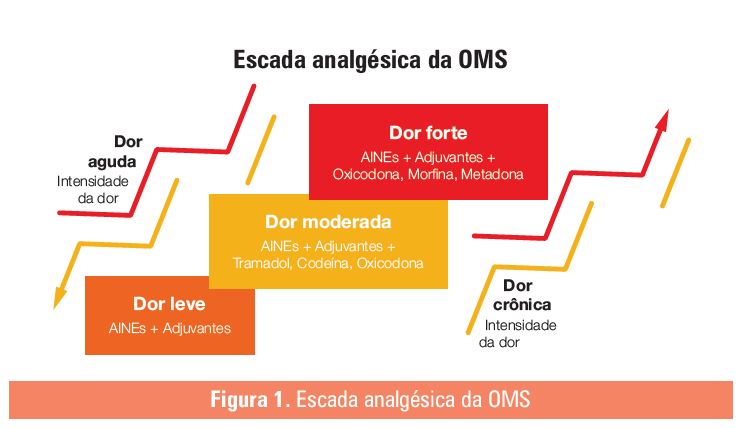
Os opioides, antes basicamente indicados para dor oncológica ou paciente terminal, atualmente têm sido usados no controle de dor moderada ou forte, aguda ou crônica, independentemente da etiopatogenia ou da possibilidade de cura da lesão ou doença de base, especialmente a partir de 1986, quando a Organização Mundial de Saúde (OMS) introduziu a escada analgésica (Fig. 1), que, embora elaborada para o tratamento da dor crônica oncológica, passou a ser utilizada também no controle da dor aguda e crônica de qualquer
etiologia, expandindo a analgesia com opioides³-6.Como a oxicodona de liberação prolongada é um opioide forte, ela deve ser usada no terceiro degrau da escada analgésica, porém, por suas características de eficácia e seu perfil de segurança, seu uso também foi recomendado em doses menores ou iguais a 20 mg por dia, já no segundo degrau da escada analgésica³.
O uso de opioides potentes para tratamento da dor crônica oncológica ou não é recomendado desde que feita a prescrição cuidadosa pelo profissional e o uso responsável pelo paciente, para otimizar a relação entre benefício e efeitos colaterais, e deve seguir os seguintes princípios: preferência pela via oral, doses adequa-das em intervalos fixos, seguir a escada analgésica, uso de forma individualizada, titular a dose, prevenir, diagnosticar e tratar os efeitos colaterais. Os efeitos adversos são comuns a todos os opioides e a todos os indivíduos, porém, sua intensidade é dependente da dose e do indivíduo, ou seja, para o efeito analgésico, há bons e maus respondedores, também para os efeitos adversos há indivíduos mais e outros menos sensíveis, por causa dos vários subtipos de receptores μ e dos polimorfismos genéticos 4-8.
Quando ocorre uso prolongado desse grupo de fármacos, especialmente na dor crônica não oncológica, é necessário que o médico prescritor tenha atenção aos efeitos adversos que podem ocorrer e conhecimentos adequados sobre dependência química, tolerância e rotação dos opioides 4-6.
Como escolher o melhor opioide
A tolerância é um estado adaptativo pelo qual a exposição a um opioide induz, ao longo do tempo, alterações que resultam em diminuição da resposta a um ou mais dos efeitos desse fármaco. A tolerância aos efeitos adversos é benigna na prática clínica, porque permite que a dose diária dos fármacos opioides seja gradual- mente aumentada até que sejam atingidas as doses analgésicas eficazes, por vezes elevadas, sem efeitos adversos significativos. O único efeito colateral que não é atenuado pela tolerância é a constipação intestinal, que deve ser tratada com dieta e medicamentos desde o início da terapêutica com os opioides 1,9-11.
No entanto, também ocorre tolerância no que se refere ao efeito analgésico que, em geral, se manifesta mais lentamente do que a tolerância aos efeitos adversos, motivo pelo qual é necessário o aumento gradual e pau-latino da dose à medida que a dor não é controlada pela dose de opioide que havia sido titulada como eficaz.
Muitas vezes é necessário aumentar a dose já estabelecida do opioide por causa de aumento da intensidade do estímulo dolorosa devido à progressão da doença, e não à diminuição de eficácia do fármaco opioide por causa da tolerância 1,9-11.
A tolerância nada tem a ver com dependência e não se verifica apenas para os opioides, pois pode ocorrer com praticamente todos os psicofármacos. A dependência física significa apenas que pode ocorrer síndrome de abstinência em caso de suspensão ou redução súbita do fármaco, e a dependência psicológica consiste no comportamento compulsivo de busca pelo opioide sem qualquer razão relacionada à dor 1,9-12.
Entretanto, como está bem estabelecido que a tolerância à analgesia pode ocorrer durante o tratamento da dor com qualquer opioide, o médico deve aumentar gradativamente a dose diária para garantir a analgesia adequada e ter atenção à progressão dos efeitos adversos, que podem ser tão intensos que inviabilizam o uso daquele opioide. Portanto, para poder garantir analgesia adequada para o paciente, o médico deve ter sempre em mente a necessidade de fazer a rotação do opioide 12.
Rotação Opioide
Rotação opioide é a mudança de fármaco ou de via de administração com o objetivo de melhorar os resultados, ou seja, é a troca de um opioide por outro quando a analgesia é inadequada e/ou os efeitos colaterais relacionados devidos ao opioide são incontroláveis 11,13-18.
Na prática, a rotação de opioide implica em mudar de um opioide para outro com o objetivo de controlar melhor a dor ou reduzir a disfunção cognitiva, as alucinações, o delírio, as mioclonias, as náuseas e vômitos, a constipação e a hipotensão ortostática, que são os principais efeitos adversos que ocorrem quando são usadas doses altas de opioides por período prolongado 19,20.
As principais indicações para a rotação do opioide são a redução da capacidade analgésica pelo agravamen-to da situação subjacente em paciente tratado com opioides fracos, desenvolvimento de tolerância ou hiperal-gesia induzida por opioide, diminuição da absorção do opioide, interação com outros fármacos, acumulação de metabólitos, redução da função renal, preço ou falta do fornecimento do opioide 16.
Riscos associados à rotação de opioides
Geralmente a rotação de opioides tem vantagens significativas para o controle da dor dos pacientes com dor crônica, no entanto, é necessário estar alerta para os riscos associados a esta estratégia, uma vez que podem ocorrer erros grosseiros de sub ou sobredosagem quando é realizada a conversão de um opioide para outro, pois a sobredosagem pode desencadear efeitos adversos eventualmente graves e mesmo fatais, por outro lado, a dose baixa em excesso vai agravar a dor, podendo até desencadear síndrome de abstinência devido à redução rápida da dose de opioide 21.
Nenhuma tabela de equivalência entre opioides deve ser utilizada sem avaliação cuidadosa e sistemática do paciente ao mudar de um opioide por outro, tendo sempre em mente que pode haver tolerância cruzada in- completa entre opioides, possibilidade de polimorfismos genéticos que podem alterar significativamente a resposta a um dos opioides e também falência de via de administração, de metabolização ou de elimina-ção 1,21.
Dose equianalgésica
A dose equianalgésica ou equipotente de um opioide é a dose que produz analgesia equivalente em relação ao composto de referência, que geralmente é a morfina, permitindo obter uma relação de dose de modo que os dois opioides proporcionem aproximadamente o mesmo alívio da dor. A dose equianalgésica que deve ser utilizada na rotação de opioides deve levar em consideração o contexto clínico, não podendo ser feita sem conhecimento adequado dos quocientes de conversão utilizados 22,23.
A equianalgesia entre dois fármacos opioides não pode ser considerada um simples cálculo matemático, porque varia de acordo com o sexo, as disfunções dos diversos órgãos, a presença de interações farma-cológicas, as diferenças individuais da farmacocinética e farmacodinâmica 22.
Cálculo da dose do novo opioide
Uma diretriz fundamental a ser respeitada na rotação de opioides é que a dose ótima do opioide para cada paciente é determinada por titulação, sendo que as tabelas de equianalgesia ou de conversão (Tabela 1) devem ser consideradas apenas como ferramenta útil para definir uma dose inicial criteriosa do novo opioide 22,23.
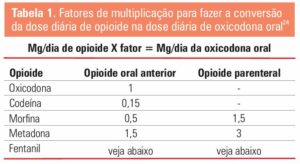
Conversão de fentanil transdérmico para comprimidos de cloridrato de oxicodona de liberação prolongada: 18 horas após a eliminação do adesivo transdérmico de fentanil, pode-se iniciar o tratamento com cloridrato de oxicodona. Cada 25 mcg de fentanil transdérmico corresponde a 10 mg de cloridrato de oxicodona de liberação prolongada 24 .
A mudança da via de administração para um mesmo opioide, embora não seja considerada exatamente uma conversão de opioide, deve levar em consideração a equianalgesia, pois pode ocorrer eventual alteração da biodisponibilidade do fármaco, em termos de hidro e lipossolubilidade, que possibilitam a absorção no trato
gastrointestinal ou a absorção sublingual e transdérmica, evitando ou não o efeito de primeira passagem 19,23,25.
A dose do opioide que será usado em substituição ao opioide em uso deve ser calculada considerando a tolerância cruzada incompleta, sendo mais seguro reduzir em 25 a 50% a dose diária do novo opioide
19, calculada por meio das tabelas de equianalgesia ou de conversão 20,25.
Outro fator que deve ser respeitado são as diferenças farmacodinâmicas entre o opioide em uso e o novo opioide, especialmente fatores que possam interferir na bio-disponibilidade, isto é, na quantidade do fármaco que chega aos receptores, e também dos polimorfismos genéticos responsáveis por resposta diferente a cada opioide 19,23,25.
Os pacientes devem ser avaliados cuidadosamente quanto à idade, ao sexo, à raça, às interações farmaco-lógicas, comorbidades, além da resposta prévia do paciente ao uso anterior de opioide no que diz respeito à eficácia e tolerabilidade, via de administração, disponibilidade do novo opioide e se a rotação do opioide é realizada em paciente internado ou ambulatorial 19,20,23,25.
Para calcular a dose diária total de opioide, é necessário considerar a dose do opioide usada pelo paciente em 24 horas, incluindo a dose do opioide de resgate utilizada para controlar a dor irruptiva. Com base na tabela de equianalgesia, é calculada a dose diária total equivalente de morfina e, com base na dose diária total equivalente de morfina, é calculada a dose total diária do novo opioide, que deve ser reduzida em 25 a 50%, considerando o estado clínico do paciente, bem como a dose e a duração do tratamento com o opioide que será trocado 19,20,23,25.
Essa redução é feita devido à variabilidade individual, à tolerância cruzada incompleta e considerando ainda algumas situações de risco, como idade avançada e insuficiência hepática e/ou renal. Maiores reduções de dose são recomendadas para pacientes idosos, pacientes com doença cardiopulmonar, hepática ou renal graves, quando a dose do opioide que será substituído é muito alta e quando o paciente pode ser mais sensí- vel ao opioide por não ser caucasiano. Se necessário fazer arredondamento da dose, deve ser usada a dose
mais baixa 19,20,23,25.
Conclusões
A rotação de opioide tem como objetivo melhorar o controle da dor ao aprimorar a analgesia e reduzir os efeitos adversos que ocorrem quando usadas doses altas de opioides por período prologado, porém, precisa ser implementada com cautela e uso de tabelas de conversão, as quais devem ser consideradas uma ferramenta útil para definir a dose inicial criteriosa do novo opioide.
REFERÊNCIAS
1. Webster LR, Fine PG. Review and critique of opioid rotation practices and associated risks of toxicity. Pain Med. 2012;13:562-70.
2. Pergolizzi JV, Paladini A, Varrassi G, et al. Change Pain: Ever Evolving-An Update for 2016. Pain Ther. 2016;5:127-33.
3. Maltoni M, Scarpi E, Modonesi C, et al. A validation study of the WHO analgesic ladder: a two-step vs three-step strategy. Support Care Cancer. 2005;13:888-94.
4. Trescot AM, Boswell MV, Atluri SL, et al. Opioid guidelines in the management of chronic non-cancer pain. Pain Physician. 2006;9:1-39.
5. Furlan AD, Sandoval JA, Mailis-Gagnon A, et al. Opioids for chronic pain: a meta-analysis of effectiveness and side effects. CMAJ. 2006;174:1589-94.
6. Quigley C. Opioid switching to improve pain relief and drug tolerability. Cochrane Database Syst Rev. 2013;18:CD004847.
7. Kalso E, Edwards JE, Moore RA, et al. Opioids in chronic non-cancer pain: systematic review of efficacy and safety. Pain. 2004;112:372-80.
8. Pergolizzi J, Böger RH, Budd K, et al. Opioids and the management of chronic severe pain in the elderly: consensus statement of an International Expert Panel with focus on the six clinically most often used World Health Organization Step III opioids (buprenorphine, fentanyl, hydromorphone, methadone, morphine, oxyco-done). Pain Pract. 2008;8(4):287-313.
9. Fraser HF. Tolerance to and physical dependence on opiates, barbiturates, and alcohol. Annu Rev Med. 1957;8:427-40.
10. Uniyal A, Gadepalli A, Akhilesh, et al. Underpinning the Neurobiological Intricacies Associated with Opioid Tolerance. ACS Chem Neurosci. 2020;11:830-9.
11. Kraychete DC, Sakata RK. Uso e rotação de opioides para dor crônica não oncológica. Rev Bras Anestesiol. 2012;62:554-62.
12. Rosenblum A, Marsch LA, Joseph H, et al. Opioids and the treatment of chronic pain: controversies, current status, and future direc-tions. Exp Clin Psychopharmacol. 2008;16:405-16.
13. Quang-Cantagrel ND, Wallace MS, Magnuson SK. Opioid substitution to improve the effectiveness of chronic noncancer pain control: A chart review. Anesth Analg. 2000;90:933-7.
14. Mercadante S, Bruera E. Opioid switching: A systematic and critical review. Cancer Treat Rev 2006 ;32:304-15.
15. Riley JL, Ross JR, Rutter D, et al. No pain relief from morphine? Individual variation in sensitivity to morphine and the need to switch to an alternative opioid in cancer patients. Support Care Cancer. 2006;14:56-64.
16. Fine PG, Portenoy RK. Ad Hoc Expert Panel on Evidence Review and Guidelines for Opioid Rotation. Establishing “best practices” for opioid rotation: Conclusions of an expert panel. J Pain Symptom Manage. 2009;38:418-25.
17. Mercadante S, Ferrera P, Villari P, et al. Frequency, indications, outcomes, and predictive factors of opioid switching in an acute palliative care unit. J Pain Symptom Manage. 2009;37:632-41.
18. González-Barboteo J, Trelis-Navarro J, Tuca-Rodríguez A, et al. Rotación de opioides: una alternativa en el tratamiento del dolor refractario en pacientes con cancer. Med Clin (Barc). 2010;135:617-22.
19. Souter KJ, Fitzgibbon D. Equianalgesic dose guidelines for long-term opioid use: Theoretical and practical considerations. Sem Anesth Perioper Med Pain. 2004;23:271-80.
20. Anderson R, Saiers JH, Abram S, et al. Accuracy in equianalgesic dosing: Conversion dilemmas. J Pain Symptom Manage. 2001;21:397-406.
21. International Association for the Study of Pain. Rethinking Opioid Equivalence. Pain Clinical Updates. 2002; 4(10). Disponível em: https://s3.amazonaws.com/rdcmsiasp/ files/production/public/FileDownloads/ClinicalUpdates/PCU%20Volume%20X%20Issue%204.pdf. Acessado em 01/04/2020.
22. Shaheen P, Walsh D, Lashenn W, et al. Opioid Equianalgesic Tables: Are they all equally dangerous? J Pain Symptom Manage. 2009;38:409-17.
23. Mercadante S, Caraceni A. Conversion ratios for opioid switching in the treatment of cancer pain: a systematic review. Palliat Med. 2011;25:504-15.
24. Bula do Produto Oxypynal. Disponível em: http://www.anvisa.gov.br/datavisa/fila_bula/index.asp. Acessado em 15/04/2020.
25. Gammaitoni AR, Fine P, Alvarez N, et al. Clinical application of opioid equianalgesic data. Clin J Pain 2003;19:286-97.

Sorry, the comment form is closed at this time.